Questa esperienza ci permette di osservare sperimentalmente, a temperature relativamente basse, il passaggio di stato dell’acido stearico, da solido a liquido e viceversa, ovvero la sua fusione e la sua solidificazione.
L’acido stearico, dal greco stéar, che significa sego (grasso di manzo) è un acido grasso saturo a catena lunga (da 14 a 18 atomi di carbonio), con peso molecolare di 284,47 dalton. In forma purificata si presenta sotto forma di fiocchi bianchi e lucenti o polvere, pochissimo solubile in acqua, con punto di fusione a 69-70 °C e di ebollizione a 383 °C.
L’acido stearico si ritrova come estere del glicerolo nei grassi ed oli animali e vegetali, dove è uno dei più comuni acidi grassi a catena lunga. E’ usato come ingrediente nella produzione di candele, saponi, plastica, pastelli ad olio, lubrificanti, cosmetici e come ammorbidente nelle gomme da masticare. Il suo nome IUPAC è acido ottadecanoico con formula bruta molecolare C18H36O2 e la struttura semplificata è rappresentata nella figura di seguito riportata, (ogni vertice rappresenta un atomo di carbonio legato agli atomi di idrogeno omessi).
Materiale
- Termometro portata 150°C e sensibilità di 1°C;
- Sostegno metallico con pinza per provettoni;
- Becher da 500 ml;
- Piastra termica possibilmente con agitatore magnetico integrato;
- Cronometro;
- Provettone 20×200;
- bacchetta di vetro.
Sostanze utilizzate
- Acido ottadecanoico o stearico;
- Acqua distillata.
Valutazione dei rischi
L’esperienza va eseguita con molta attenzione e impiegando i dispositivi di protezione individuali come il camice, guanti termici e occhialetti. La piastra termica raggiunge temperature elevate e nel caso si dovesse accidentalmente toccarla, porre la parte ustionata immediatamente sotto un getto di acqua fredda di rubinetto. Attenzione anche all’acqua calda presente nel becker verso la parte terminale dell’esperienza usando, qualora si dovesse spostare il becher caldo, un paio di guanti termici di protezione. L’acido stearico o ottadecanoico non è pericolosa secondo la Direttiva 67/548/CEE, ma comunque si linka la scheda di sicurezza cliccando sulla sostanza.
Procedimento per la curva di riscaldamento
- Sistemare su di una piastra termica un becker da 500 ml riempito fino a 3/4 con acqua distillata o di rubinetto;
- Immergere, a bagno maria, un provettone 20×200 contenente qualche grammo di acido stearico puro;
- Introdurre nel provettone un termometro facendo penetrare completamente il bulbo nella polvere dell’acido stearico;

Allestimento per la determinazione della curva di riscaldamento dell’acido stearico - Accendere la piastra termica, agitare con una bacchetta l’acqua (se non si ha a disposizione dell’agitazione magnetica) e contemporaneamente far partire il cronometro;
- Leggere la temperatura ogni 60 secondi, senza mai fermare il cronometro, riportando i valori su di una tabella;
- Annotare, oltre al tempo e alla temperatura, lo stato fisico dell’acido ottadecanoico (se solido o liquido);
- Raggiunti circa i 45°C, si può misurare la temperatura ogni 30 secondi, fino a raggiungere i 70°C;
- Fare molta attenzione quando avviene il passaggio di stato ovvero quando si ha la “fusione”, riportando in tabella il momento in cui si verifica e quando la polvere dell’acido stearico è completamente fusa;

Fase iniziale della fusione (presenza di poco liquido e molto solido) 
Fase intermedia della fusione (presenza di molto liquido e poco solido) - Dopo che la temperatura supera i 70°C, misurarla di nuovo ogni 60 secondi fino ad arrivare a circa 95°C.
Procedimento per la curva di raffreddamento
- Continuando l’esperienza, alzare il provettone contenente l’acido stearico dal bagno maria ormai bollente e annotare, in una nuova tabella, il tempo iniziale, la temperatura e lo stato fisico;
- Leggere sul termometro la temperatura ogni 60 secondi fino ad arrivare a temperatura ambiente o almeno a 40°C;
- Verificare quando avviene il passaggio di stato dell’acido stearico ovvero quando si ha, questa volta, la solidificazione;

Inizio solidificazione a circa 67°C - Riportare in tabella a quale temperatura inizia la solidificazione e quando essa termina.
Tabella e grafici
Con i dati ottenuti si dovrà realizzare un grafico su carta millimetrata o su computer con un software dedicato. Nel primo caso si sfrutterà tutta la superficie del foglio A4, meglio però utilizzare il formato A3. Sulle ascisse va riportato l’asse del tempo in secondi e sulle ordinate l’asse della temperatura in gradi centigradi (°C). L’intervallo da considerare è di 1 cm per ogni sessanta secondi per il tempo e 2 cm ogni 10°C per la temperatura; il tutto va raddoppiato se si utilizza un foglio di carta millimetrata con formato A3.
| TABELLA DEI DATI PER LA CURVA DI RISCALDAMENTO | ||
| Tempo (min) | Temperatura (°C) | Stato fisico (S=solido; L=liquido) |
| 0 | 22 | S |
| 1 | 26 | S |
| 2 | 30 | S |
| 3 | 34 | S |
| 4 | 36 | S |
| 5 | 41 | S |
| 6 | 45 | S |
| 7 | 46 | S |
| 8 | 49 | S |
| 9 | 52 | S |
| 10 | 55 | S |
| 11 | 57 | S |
| 12 | 60 | S |
| 13 | 67 | S>L |
| 14 | 67 | L>S |
| 15 | 68 | L |
| 16 | 70 | L |
| 17 | 76 | L |
| 18 | 82 | L |
| 19 | 91 | L |
| 20 | 96 | L |
| TABELLA DEI DATI PER LA CURVA DI RAFFREDDAMENTO | ||
| Tempo (min) | Temperatura (°C) | Stato fisico (S=solido; L=liquido) |
| 0 | 97 | L |
| 1 | 91 | L |
| 2 | 76 | L |
| 3 | 72 | L |
| 4 | 69 | L |
| 5 | 68 | L |
| 6 | 67 | L>S |
| 7 | 67 | L>S |
| 8 | 67 | L=S |
| 9 | 67 | S>L |
| 10 | 67 | S>L |
| 11 | 67 | S>L |
| 12 | 67 | S>L |
| 13 | 65 | S |
| 14 | 60 | S |
| 15 | 55 | S |
| 16 | 50 | S |
| 17 | 45 | S |
| 18 | 39 | S |
| 19 | 32 | S |
| 20 | 22 | S |
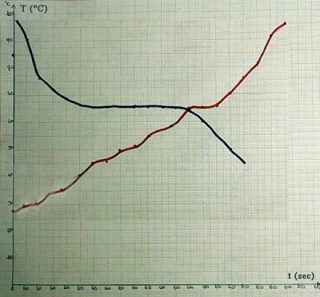
Il grafico in figura rappresenta l’andamento della curva di riscaldamento (in rosso) dell’acido stearico e la curva di raffreddamento (in blu).
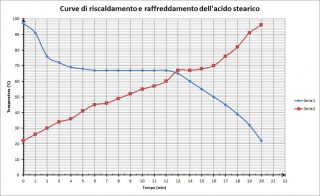
Osservazioni
L’esperienza potrebbe non riuscire perfettamente perché il procedimento avviene in un sistema termodinamico aperto ovvero con flussi di energia e massa scambiati con l’ambiente esterno. Il calore prodotto dalla piastra termica proviene dal basso e si propaga verso l’alto e non è distribuito in maniera omogenea. L’uso di dispositivi più raffinati, (purtroppo costosi), darebbero risultati sicuramente più attendibili. Ad esempio, l’utilizzo di un mantello riscaldante con agitatore magnetico integrato al posto della piastra termica potrà essere una delle soluzioni per migliorare la prova.
Nonostante l’inconveniente di non poter creare un sistema ideale, i dati che si possono ottenere con questa esperienza, si avvicinano in maniera soddisfacente a quelli teorici soprattutto nel caso della curva di raffreddamento. Infatti la perdita di calore avviene in modo più graduale rispetto al riscaldamento e il passaggio di stato (solidificazione) impiega un tempo maggiore rispetto a quello della fusione, come si può vedere dal grafico sopra.
La sosta termica è più evidente nella curva di raffreddamento che in quella di riscaldamento per i motivi prima esposti e in questo caso avviene alla temperatura di circa 67°C.






quale software è stato utilizzato per fare la tabella sulla curva di riscaldamento?
Salve, la tabella è stata creata con un software integrato nell’editor del sito, ma per realizzarla si può utilizzare word, excel, libreoffice writer ecc..