Le molecole possono avere o meno una certa polarità dovuta ad una distribuzione non omogenea degli elettroni di legame. Questi, infatti, possono essere attratti più o meno fortemente dagli atomi coinvolti nei legami chimici e formare delle parziali cariche positive su una parte della molecola e delle parziali cariche negative nella parte opposta, creando così un dipolo elettrico. La tendenza di un atomo ad attrarre su di se gli elettroni di legame è detta elettronegatività ed il valore è riportato nella tavola periodica. Valori crescenti di elettronegatività indicano un alto potere attrattivo nei confronti degli elettroni di legame e valutando le differenze di elettronegatività fra atomi impegnati in un legame, si potrà determinare quale parte della molecola presenterà una parziale carica negativa (δ-) e quale altra presenterà parziale carica positivà (δ+). Nel caso della molecola d’acqua, essendo l’atomo di ossigeno più elettronegativo dell’idrogeno, si avrà un’addensamento degli elettroni di legame più verso l’atomo d’ossigeno e meno sugli idrogeni, conferendo così polarità alla molecola.

Si può osservare il comportamento di un flusso di acqua distillata quando vi si avvicina una bacchetta di bachelite elettrizzata. Questa, infatti, dopo averla strofinata con uno straccio di lana si caricherà negativamente e il flusso verrà attratto come nella figura.

Da notare inoltre che, se si avvicina una bacchetta di vetro carica positivamente il flusso di acqua verrà, anche in questo caso, attratto. La causa di ciò è che le molecole d’acqua si comportano come dei dipoli e si orientano in modo tale da mostrare la carica di segno opposto al campo elettrostatico generato dalla bacchetta elettrizzata.

Nel caso dei liquidi apolari, il flusso non viene deviato dalla bacchetta elettrizzata proprio perchè questi non si comportano da dipoli e le molecole non risentono del campo elettrico.

Infatti, nel caso in cui, in una molecola la differenza di elettronegatività tra i due atomi in oggetto è nulla, la molecola è apolare. Consideriamo ad esempio la molecola di azoto in cui sono presenti due atomi di azoto N-N uniti da un legame covalente puro; si noterà che essendo costituita da due identici elementi, la differenza di elettronegatività è zero e quindi anch’essa apolare. Tuttavia una molecola può avere legami polari ma essere una molecola apolare. Se i legami polari sono uniformemente ovvero simmetricamente distribuiti, i dipoli si annullano reciprocamente e la molecola è apolare. Consideriamo, ad esempio, l’anidride carbonica in cui il legame tra il carbonio e ciascun atomo di ossigeno è polare a causa della differenza di elettronegatività tra i due elementi ma, essendo la molecola simmetrica, il baricentro delle cariche positive e il baricentro delle cariche negative coincidono e i due momenti dipolari si compensano e quindi la molecola risulterà apolare.
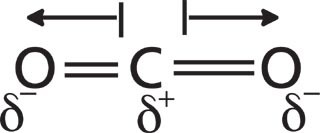
Nell’esperienza che segue si utilizzeranno sostanze apolari e polari che dovranno essere testate per individuare a quale gruppo appartengono ed elencarle nella tabella.
L’obiettivo dell’esperienza di laboratorio è quindi verificare se un liquido sia polare o meno in base al comportamento del flusso del liquido stesso in presenza di un campo elettrostatico.
Materiale occorrente: burette da 50 ml con sostegno metallico, becker da 100 ml, bacchetta di vetro e di bachelite, panno di lana.
Liquidi da testare: acqua distillata, etanolo puro, n-decano, acido oleico, acido lattico.
Valutazione dei rischi: per i liquidi impiegati leggere attentamente le schede di sicurezza sopra linkate. Lavorare sotto cappa aspirante e usare i D.P.I. che in questo caso sono: camice, guanti e occhialetti. Eseguire l’esperienza solo in presenza degli insegnanti.
Procedimento:
- Versare in ogni buretta circa 50 ml di un liquido da testare;
- Porre sotto il becco della buretta un becker vuoto da 100 ml;
- Strofinare, per circa un minuto, la bacchetta di bachelite con un panno di lana;
- Dopo aver aperto il rubinetto della buretta contenente il liquido da testare avvicinare al flusso la bacchetta elettrizzata;
- Annotare se il flusso viene deviato o meno;
- Effettuare la stessa prova per ogni liquido in esame;
- Ripetere le stesse procedure utilizzando, questa volta, una bacchetta di vetro;
- Recuperare i liquidi utilizzati per successivi esperimenti ed ulteriori prove.
Tabella da completare :
| SOSTANZA LIQUIDA | APOLARE | POLARE |
| Acqua distillata | ||
| Etanolo puro | ||
| n-decano | ||
| Acido oleico | ||
| Acido lattico |
Osservazioni: Dopo aver disegnato le formule di struttura di ogni sostanza in esame, scrivere le opportune considerazioni in funzione di quello che in teoria dovrebbe risultare riguardo la polarità o meno e ciò che si è verificato durante l’attività sperimentale. Nel caso dell’acido oleico infatti, pur essendo una molecola contenente dei legami polari e asimmetrica, probabilmente non si noterà deviazione del flusso. Spiegare perchè.


Con questo principio si potrebbero respingere le particella di saliva ?(aerosol)
Salve, grazie per la partecipazione e la lettura dell’articolo in oggetto, che spero sia stato d’aiuto per comprendere meglio l’argomento trattato. Alla domanda fatta credo che non sia possibile evitare le particelle di saliva proprio perchè questa è costituita per la maggior parte da acqua (circa il 98%) e da altri sali disciolti in piccole quantità. Se si carica elettrostaticamente il tessuto della mascherina, le particelle di saliva addirittura potrebbero essere attratte proprio perchè l’acqua è polare. Quindi eviterei tale operazione. Grazie
Interessante esposizione. Quale potrebbe essere una applicazione pratica di questo tipo di comportamento di un fluido in genere, in campo tecnologico.
Grazie
Salve, interessante domanda e navigando su internet ho scoperto che alcune sostanze polari e apolari sono impiegate come dielettrici nei condensatori per indebolire il campo elettrico preesistente, vedi “http://www.openfisica.com/fisica_ipertesto/openfisica4/polari.php”. Molto interessante è anche l’impiego di queste molecole nel campo degli adesivi che permettono, in funzione dei legami chimici coinvolti (van der Waals o a ponte d’idrogeno), incollaggi strutturali, vedi “https://books.google.it/books?id=gxGJAgAAQBAJ&pg=PA37&lpg=PA37&dq=molecole+polari+in+campo+tecnologico&source=bl&ots=_YCoyM8gSC&sig=IPMFoDfgWR6vEB56hAC4zVDcRto&hl=it&sa=X&ved=0ahUKEwiOxtmrtNTKAhUBRg8KHZl8CAQQ6AEIOjAF#v=onepage&q=molecole%20polari%20in%20campo%20tecnologico&f=false”