La titolazione, in questa circostanza, è una tecnica che ci permette di determinare la concentrazione di una soluzione di un acido forte, sfruttando una soluzione di una base forte di cui è nota la sua concentrazione. Ovviamente è possibile anche il contrario, ovvero determinare la concentrazione incognita di una base forte utilizzando una soluzione a titolo noto di un acido forte. Questa tecnica è adottata anche in diverse altre applicazioni come ad esempio nell’argentometria, nella permanganometria, nella complessometria ed altro. Nel nostro caso affronteremo un esempio molto semplice di titolazione per capirne meglio il funzionamento, tralasciando per il momento, le altre più complicate e difficili nell’esecuzione.
Per comprendere meglio il principio su cui si basa la titolazione acido-base forte, dovremmo affrontare prima alcune considerazioni teoriche riguardo il concetto di “punto di equivalenza” e come agiscono gli “indicatori di pH”.
La reazione chimica che si sfrutta è quella di neutralizzazione tra un acido e una base forte e nella esperienza proposta verrà utilizzato acido cloridrico e idrossido di sodio. Come si può notare dall’equazione chimica, un certo numero di moli dell’acido reagirà con lo stesso numero moli di base per avere come prodotti acqua e cloruro di sodio in soluzione.
HCl(sol) + NaOH(sol) → H2O + NaCl (sol)
Dovendo titolare una soluzione di acido cloridrico, dovremmo utilizzare una soluzione a concentrazione nota di idrossido di sodio. La condizione che ci permetterà di stabilire la concentrazione incognita dell’acido dovrà essere ovviamente quella di individuare quante moli di NaOH, contenute in un certo volume, saranno necessarie per neutralizzare completamente tutto l’HCl presente in un determinato volume di soluzione.
Tale condizione può essere ottenuta attraverso la misurazione continua del pH della soluzione da titolare che in questo caso è dell’acido cloridrico. Infatti, aggiungendo, goccia a goccia, una soluzione di NaOH, il pH della soluzione di HCl aumenterà fino a raggiungere la neutralità, condizione detta “punto di equivalenza”. In questa situazione il numero di moli di NaOH sarà equivalente al numero di moli di HCl e sarà possibile, attraverso opportuni calcoli, determinare la concentrazione dell’acido cloridrico.
Per raggiungere il punto di equivalenza sarà necessario osservare la variazione di pH attraverso uno strumento detto pHmetro oppure, più semplicemente, sfruttando le proprietà di un indicatore di pH. Quest’ultimo non è altro che una particolare sostanza che ha la caratteristica di variare la sua colorazione in funzione della concentrazione degli ioni idrogeno, (H3O+), presenti nella soluzione da titolare. Ad ogni tonalità di colore corrisponderà un certo valore di pH e il momento in cui si avrà la condizione di equivalenza, ovvero a pH intorno 7 (neutro), la sostanza indicatore varierà la sua tonalità da un certo colore ad un altro. Le colorazioni che possono assumere queste sostanze sono però differenti a seconda della natura della sostanza stessa e sarà necessario scegliere l’indicatore che sia in grado di subire modifiche del colore facilmente osservabili. Per individuare l’indicatore di pH che può essere impiegato in una titolazione acido-base si possono consultare delle apposite tabelle dove sono riportati i campi di pH in cui l’indicatore cambia colore, detti “intervalli di viraggio”. Nel caso della titolazione di una soluzione di acido cloridrico, di cui non si conosce la concentrazione, con una soluzione a titolo noto di idrossido di sodio, può essere utilizzata una soluzione di fenolftaleina che in soluzione acida risulta incolore e in soluzione leggermente basica rosa, fino a diventare viola a pH più alcalini.
Vediamo ora un esempio di titolazione acido-base forte.
TITOLAZIONE DI UNA SOLUZIONE DI HCl CON NaOH 0,1M
Obiettivo:
Determinare la concentrazione molare di una soluzione di acido cloridrico utilizzando una soluzione di idrossido di sodio 0,1M
Materiale:
- Buretta da 50ml con divisioni da 0,1ml; LINK PER L’ACQUISTO
- Beuta da 100ml;
- Imbuto di vetro;
- Becher da 100ml;
- Foglio di carta bianca.
Reagenti:
- Soluzione standardizzata o normex di NaOH 0,1M;
- Soluzione idroalcolica di fenolftaleina allo 0,1%;
- 20ml di HCl a concentrazione incognita;
- Acqua distillata.
Valutazione dei rischi:
Sebbene si utilizzino delle soluzioni diluite (circa 0,1 M) di acido cloridrico e di idrossido di sodio è sempre meglio adottare i dispositivi di protezione individuali previsti dalle norme. Nel nostro caso è indicato l’uso di un camice, dei guanti e degli occhialetti di protezione. Lavorare sotto cappa d’aspirazione e in presenza degli insegnanti. Si linkano le schede di sicurezza cliccando sul nome dei reagenti presenti in questo paragrafo.
Procedimento:
- Con circa una ventina di millilitri di NaOH 0,1M, avvinare una buretta pulita da 50ml;
- Riempire la buretta, portando allo zero, con 50ml di NaOH 0,1M;
- In una beuta versare 20ml precisi di HCl, a concentrazione incognita, utilizzando una buretta;
- Versare, nella beuta contenente l’acido da titolare, 2 gocce di una soluzione idroalcolica di fenolftaleina allo 0,1%;
- Porre un foglio di carta bianca sotto la beuta;
- Far cadere, goccia a goccia, la soluzione di NaOH 0,1M nella beuta contenente l’acido da titolare, agitando continuamente con delicati movimenti rotatori;
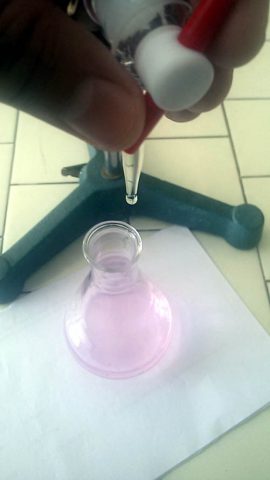
- Interrompere la titolazione non appena si individua una colorazione rosa persistente per almeno dieci secondi nella soluzione contenuta nella beuta.

Calcoli:
Per determinare la concentrazione dell’acido cloridrico incognita, si dovrà, con la titolazione, determinare il volume di NaOH 0,1M, (volume di viraggio), necessario per neutralizzare tutto l’acido cloridrico. Conoscendo il volume preciso di HCl possiamo porre come condizione nel punto di equivalenza:
n. moli di NaOH = n. moli di HCl
ed essendo il numero moli dato dal prodotto tra la molarità e il volume della soluzione:
\(n.moli=Mcdot V\)
si ha sostituendo:
M • V = M’ • V’
Dove per
- M si intende la molarità della soluzione di NaOH che nel nostro caso è di 0,1M;
- V il volume di idrossido di sodio impiegato per raggiungere il punto di viraggio;
- M’ la molarità dell’acido cloridrico incognita;
- V’ il volume di acido cloridrico utilizzato nella titolazione.
Dovendo trovare la concentrazione dell’acido cloridrico, basta isolare M′, quindi la formula da impiegare sarà:
\(M’= frac{M*V}{V’}\)
Se, ad esempio, nella titolazione acido base si impiegano 20,3 ml di NaOH 0,1M per raggiungere il punto di viraggio (soluzione rosa pallido) e se si utilizzano 20,0 ml di acido cloridrico a concentrazione incognita, il valore di molarità dell’acido sarà:
\(M’= frac{0,1mol/L*0,023L}{0,02L}\) = 0,115 mol/L
Osservazioni:
In prossimità del punto di viraggio leggere, ogni volta che si aggiunge una goccia di titolante, il volume di NaOH versato con la buretta. Nel caso in cui si oltrepassa la tonalità del rosa pallido a quella del viola, dovrà essere considerato il volume di NaOH di viraggio letto prima di aggiungere la goccia.
L’operazione di avvinamento è importante per evitare che la soluzione titolante venga ulteriormente diluita da eventuali goccioline di acqua distillata presenti all’interno della buretta non asciutta correttamente o per la presenza di eventuali sostanze inquinanti. E’ bene quindi lavare almeno tre volte la buretta con un po’ di soluzione titolante prima di riempirla definitivamente con l’NaOH 0,1M.
La soluzione di acido cloridrico di cui si dovrà determinare la concentrazione molare non deve essere molto diversa dalla concentrazione molare del titolante (NaOH) per evitare di incorrere in errori troppo elevati.

