In alcune attività di laboratorio è necessario dover utilizzare delle soluzioni molto diluite che possono raggiungere concentrazioni talmente basse che non è possibile prepararle pesando direttamente il quantitativo necessario di soluto, come avviene nell’esperienza “Preparazione di una soluzione a concentrazione nota“. Infatti potrebbe capitare di dover sciogliere, ad esempio, 0,000000015 g di un sale in 100 ml di acqua distillata. E’ evidente che neanche la bilancia analitica, che al massimo può avere una risoluzione di 0,01 mg, potrà essere utilizzata allo scopo e comunque, anche se la pesata da effettuare fosse al limite della risoluzione, si farebbe sicuramente un errore troppo elevato.
Per ovviare a tali problematiche si sfrutta il metodo delle diluizioni scalari. In questo modo si prepara una soluzione più concentrata di quella che serve e, con dei passaggi tecnici, si effettuano delle diluizioni intermedie fino a raggiungere la concentrazione desiderata. Gli inconvenienti saranno essenzialmente dovuti alle quantità di soluto e di solvente da impiegare che, per necessità, dovranno essere maggiori.
Vedremo in seguito un’esperienza che utilizza il metodo delle diluizioni scalari per ottenere una soluzione a bassissimo contenuto di soluto.
Obiettivo
Preparazione di 10 ml di una soluzione di solfato rameico (CuSO4) alla concentrazione 10-4M a partire da una soluzione di CuSO4 1M .
Materiale
- Provette di vetro 16×160 con portaprovette;
- Pipetta graduata da 10 ml con propipetta;
- Pipetta graduata da 1 ml con propipetta o contagocce;
- Pipetta pasteur;
- Becher da 50 ml;
- Beutina da 50 ml.
Sostanze
- Solfato rameico anidro CuSO4 ;
- Acqua distillata.
Valutazione dei rischi
L’esperienza non evidenzia grosse difficoltà e non richiede particolari accorgimenti tranne che per l’uso del camice e di occhiali di protezione. Attenzione però al solfato rameico di cui si allega la scheda di sicurezza cliccando sul link.
Procedimento
- Versare qualche ml della soluzione di CuSO4 1M in una beutina da 50ml e a partire da questa si effettueranno le diluizioni;
- Allestire un portaprovette con quattro provette 16×160 numerandole da 1 a 4;
- Versare in ogni provetta 9 ml di acqua distillata con una pipetta graduata da 10 ml, prelevandola da un becher da 50 ml;
- Con una pipetta graduata da 1ml o in alternativa un contagocce, versare 1 ml o 20 gocce (≅ 1 ml) di soluzione iniziale di CuSO4 1M nella prima provetta contenente i 9ml di acqua distillata, per effettuare la prima diluizione 1:10;

Trasferimento della soluzione di solfato rameico 1M nelle provette - Mescolare bene utilizzando la stessa pipetta aspirando e facendo defluire il liquido almeno tre volte nella stessa provetta;
- Prelevare di nuovo 1 ml della soluzione di CuSO4 diluito 1:10 e versarlo nella seconda provetta contenente i 9 ml di acqua distillata per ottenere CuSO4 diluito 1:100;
- Ripetere il passaggio precedente per la terza e quarta provetta fino a raggiungere la diluizione della soluzione di CuSO4 1:10000 ovvero la concentrazione di 10-4 M.

Risultato finale delle diluizioni scalari del solfato rameico 1M
Schema illustrato
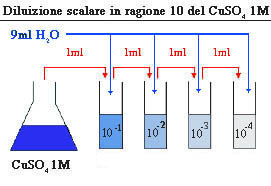
Osservazioni
Con questi metodi è possibile ottenere diluizioni infinitesime della soluzione iniziale e spesso sono utilizzati in campo farmaceutico e nella preparazione di prodotti omeopatici. Si possono comunque compiere anche altri tipi di diluizioni scalari cambiandone il fattore. Ad esempio potremmo sfruttare il fattore di diluizione 2 anziché 10 e le soluzioni risultanti avranno una scalarità del tipo, 1:2, 1:4, 1:8, 1:16, 1:32, 1:64, 1:128 e così via. Bisogna ovviamente cambiare schema tecnico adottando volumi uguali di diluente e di soluzione iniziale come si può vedere nella figura seguente.
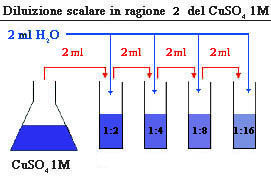
In questo modo la tonalità del colore diminuisce con minore intensità rispetto alle diluizioni scalari in ragione 10 e di conseguenza anche la concentrazione del solfato rameico. Nell’ultima provetta (diluizione 1:16) la concentrazione di CuSO4 sarà 0,0625M; valore ottenuto dal rapporto della concentrazione iniziale (1M), con il fattore di diluizione 16.



Un’altra chicca,bravo admin.