Nel 1848, un docente di chimica, Hermann von Fehling (1812-1885), del politecnico di Stoccarda, studiò e trovò un metodo per determinare qualitativamente e quantitativamente la presenza di zuccheri riducenti in un campione in esame. Molti alimenti contengono zuccheri riducenti, semplici o complessi ed è molto importante conoscerne la composizione zuccherina per avere informazioni dal punto di vista nutrizionale.
Libro consigliato: Link Laboratorio di chimica organica
Cenni teorici
Gli zuccheri possono essere classificati in riducenti e non riducenti secondo la loro capacità di ridurre particolari reattivi in ambiente basico. Il gruppo aldeidico di uno zucchero riducente viene ossidato e si forma un acido carbossilico. Affinché uno zucchero possieda attività riducente è necessario che possa esistere in una forma a catena aperta con un gruppo aldeidico o chetonico. I monosaccaridi che contengono un gruppo aldeidico sono noti come aldosi, e quelli con un gruppo chetonico sono noti come chetosi. Gli aldosi e i chetosi vengono ossidati anche se sono impegnati nel legame semiacetalico, (che si verifica durante il processo di ciclizzazione della molecola), dato che questo viene idrolizzato velocemente in ambiente basico. Gli zuccheri impegnati in legami acetalici invece, non reagiscono perché gli acetali sono stabili alle basi e non liberano l’aldeide o il chetone, sono quindi detti zuccheri non riducenti. Nella figura seguente il glucosio è ossidato ad acido gluconico.
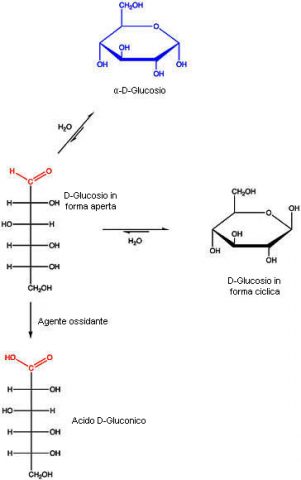
L’ossidazione avviene in ambiente basico e possono reagire anche molecole che non contengono inizialmente il gruppo aldeidico, ma che lo possono generare per isomerizzazione alcalina. È per questo motivo che danno reazione positiva non solo le aldeidi come il D-glucosio, ma anche gli α-idrossichetoni come il fruttosio che viene prima isomerizzato a glucosio e mannosio e poi, in questa forma, può essere ossidato ad acido gluconico e mannonico.
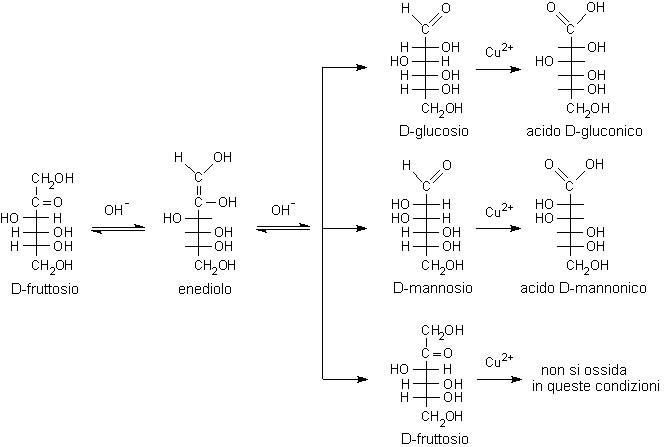
Nel caso dei disaccaridi, costituiti dall’unione di due zuccheri semplici (monosaccaridi), il legame glicosidico può interessare il carbonio anomerico di un monosaccaride e un gruppo alcolico dell’altro (come nel caso del lattosio e maltosio) o entrambi gli ossidrili anomerici, ossia quelli legati direttamente all’atomo di carbonio C1 negli aldosi e C2 nei chetosi (come nel caso del saccarosio).
Il saccarosio, infatti, è costituito dall’unione di una molecola di glucosio con una di fruttosio e il legame è di tipo 1-2 α, ß diglicosidico che interessa entrambi gli OH dei carboni anomerici. Non avendo quindi gruppi anomerici liberi, ovvero capaci di trasformarsi in gruppi carbonilici, il saccarosio è uno zucchero non riducente.
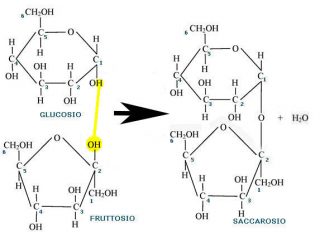
Differente è invece il caso del lattosio in cui i due monomeri, il D-glucosio e il D-galattosio, sono uniti da un legame di tipo ß 1-4, dando origine ad uno zucchero riducente in quanto è disponibile il C1 anomerico del glucosio che lo compone, per una eventuale trasformazione in gruppo aldeidico.
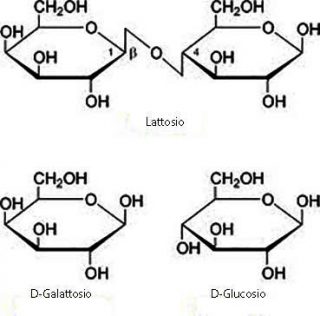
Anche nel maltosio (zucchero riducente), costituito dall’unione di due molecole di glucosio, il legame glicosidico impegna un ossidrile anomerico (C1) di un glucosio con il C4 dell’altro.
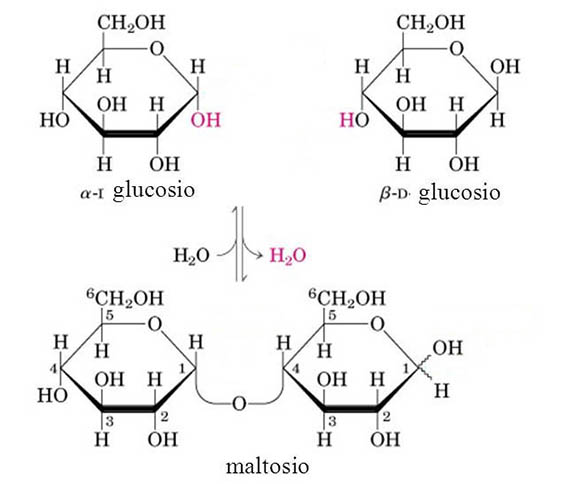
La motivazione riguardo il comportamento riducente del Maltosio e del Lattosio sta nel fatto che, in entrambi i casi, uno dei due monosaccaridi della molecola disaccaride può aprirsi per formare una catena aperta che in soluzione è in equilibrio con la forma chiusa. La catena aperta del monosaccaride coinvolto presenterà il gruppo aldeidico responsabile dell’azione riducente nei confronti dello ione rameico del reattivo di Fehling. Sotto è riportato l’equilibrio tra la forma ciclica e la forma a catena aperta del maltosio in cui viene a formarsi il gruppo aldeidico disponibile per una eventuale ossidazione.
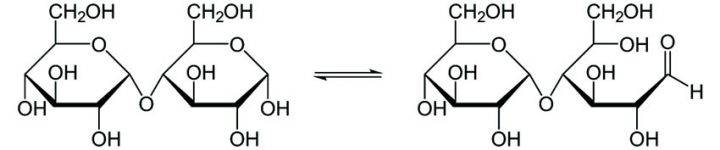
Reazione redox del reattivo di Fehling
La presenza di zuccheri riducenti negli alimenti può essere facilmente dimostrata ricorrendo alla reazione di Fehling. In questo reattivo è presente lo ione rameico (Cu++) che si riduce, in ambiente basico, a ione rameoso (Cu+), formando un precipitato di ossido rameoso (Cu2O), di colore rosso mattone. Il gruppo aldeidico dello zucchero invece, si ossida ad acido carbossilico secondo la seguente reazione redox:
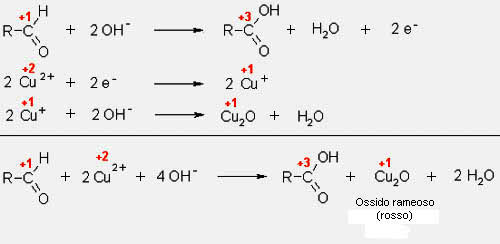
Saggio di Fehling
Obiettivo
Determinazione qualitativa degli zuccheri riducenti e non riducenti presenti in campioni di alimenti.
Materiale
- Provette di vetro;
- Piastra termica; LINK PER L’ACQUISTO
- Becker da 500mL con portaprovette per bagno maria;
- Pipette graduate da 2 mL;
- Omogeneizzatore (solo per gli alimenti solidi). LINK PER L’ACQUISTO
Reagenti
- Reattivo di Fehling;
- Acqua distillata;
- Acido acetico 6% (solo per eventuale impiego di latte come campione).
Preparazione del reattivo di Fehling
Il reattivo di Fehling non è molto stabile in quanto lo ione rameico, contenuto nella soluzione, potrebbe precipitare come idrossido per la presenza di NaOH.
Cu++ + 2 OH‾ → Cu(OH)2 ↓
Per ovviare a questo problema si preparano due soluzioni chiamate, Fehling A e B. Il rame della soluzione A viene mantenuto in soluzione come ione rameico grazie al tampone tartrato sodico potassico (Fehling B) che lo complessa, (tenendolo in soluzione), impedendo al rame di precipitare come idrossido.
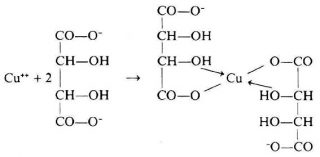
Le due soluzioni vanno conservate separatamente e al momento dell’uso si mescolano in parti uguali nella quantità necessaria per l’esperienza. Il reattivo è stabile per circa 30 minuti dalla preparazione.
- Reattivo di Fehling A: in pallone tarato da 1000 mL si sciolgono 69,28 g di solfato rameico pentaidrato (CuSO4 • 5 H2O) con acqua distillata e si porta a volume.
- Reattivo di Fehling B: in pallone tarato da 1000 mL si sciolgono 346 g di sale di Seignette (tartrato doppio di sodio e potassio) e 100 g di idrossido di sodio (NaOH) in acqua distillata; dopo dissoluzione si porta a volume.
Valutazione rischi
Si allega il link per la scheda di sicurezza del Fehling A e del Fehling B, da usare con cautela utilizzando un camice, dei guanti anti acido e occhialetti di protezione. Durante l’impiego della piastra termica usare guanti termici.
Procedimento
Per effettuare la prova qualitativa si pone in una provetta 1 mL del liquido in cui si vuol evidenziare la presenza di zuccheri e si aggiungono 2 mL del reattivo di Fehling preparato. Si scalda il tutto a bagno maria a caldo o alla fiamma per alcuni secondi.

In presenza di zuccheri il liquido assumerà una colorazione variabile tra il giallo, l’arancio ed il rosso mattone; lasciando a riposo la provetta per un po’ di tempo il colore si depositerà sul fondo sotto forma di un precipitato insolubile di composti di rame.

Osservazioni
Sarebbe opportuno eseguire il test allestendo una provetta con un campione sicuramente positivo (ad esempio una soluzione di glucosio) e un campione sicuramente negativo (come ad esempio una soluzione di saccarosio) per confrontare le colorazioni assunte con altri campioni di alimenti.
Per avere la certezza che il reattivo preparato sia efficace e non scaduto o inquinato, si può aggiungere acqua distillata al posto del campione da analizzare e verificare che non ci siano variazioni di colorazione.
I campioni da testare devono essere limpidi e nel caso dei succhi di frutta, in cui sono presenti particelle solide in sospensione, è meglio effettuare la filtrazione prima del test. Riguardo invece gli alimenti solidi è bene omogeneizzarli con acqua distillata e filtrarli. Se si vuole evidenziare la presenza di zucchero (lattosio) nel latte è bene aggiungere a 10 mL di latte tre o quattro gocce di acido acetico al 6% (oppure aceto) per far precipitare le proteine, filtrare il tutto ed utilizzare la soluzione limpida così ottenuta.
Nel caso la quantità di zuccheri presente nel campione fosse bassa il colore può diventare, invece che giallo o rosso, di un verde torbido.


ciao, ma come faccio a scaricarlo…..? non vedo dove c’è scritto….io sono una bambina….e mi interessa molto……
grazie
comunque bel lavoro
no, ottimo…..complimenti……ciao
Salve Ari, sono contento che segui i nostri articoli con interesse. Potrai trovare alla fine di ogni articolo un’icona per la stampa ed un’altra per avere l’articolo in PDF. In quest’ultimo caso è possibile evidenziare e copiare le parti utili per ritrascriverle su un programma di video-scrittura. Puoi anche usare un convertitore di formati on-line chiamato I-Love-PDF al link: https://www.ilovepdf.com/it che ti permetterà di ottenere direttamente un formato a piacere. Ricorda però che la pubblicazione di parti o di interi articoli presi dal sito “Laboratorio scolastico” sono coperti da copyright e non possono essere messi su internet senza autorizzazione del responsabile del sito Laboratorio scolastico. Grazie per i complimenti.
ciao, sono bellissime e utilissime informazioni…vorrei soltanto avere un copia e incolla….perchè così non devo copiare tutto a mano…….
grazie…..
Buon giorno, complimenti per il sito, assai ricco e ben fatto. Mi chiedevo se fosse possibile scaricare il file dell’esperienza descritta. Grazie
Grazie Laura del complimento e per la segnalazione riguardo la possibilità di scaricare il file dell’esperienza. Ho appena implementato la funzione stampa e scarica il file in PDF su ogni articolo del sito. Mi raccomando di dichiarare sempre l’origine della fonte ogni volta che esponi in pubblico ogni articolo estratto da questo sito per evitare inconvenienti di Copyright. Grazie
Bel lavoro admin, i suoi alievi dovrebbero essergli riconoscenti per aver offerto un eccellente relazione
su un argomento di sicuro interesse didattico e professionale.
Grazie elettrico, non ti nascondo che la pubblicazione dell’articolo mi ha fatto rispolverare alcune nozioni di chimica organica che feci all’università una ventina di anni fa. Queste attività fanno bene a tutti per allenare la nostra mente. LVeP (lunga vita e prosperità “L. Nimoy”)
Bello, ma c’è troppa pubblicità su questo sito.
Grazie Antonio per il complimento. Le pubblicità in questo sito, come in tutti i siti “*.altervista.org”, sono necessariamente da ospitare per poter avere a disposizione uno spazio gratuito nel server e sostenere quel minimo necessario ai costi di gestione. Comunque cercherò di inoltrare una richiesta ai gestori per ridurre almeno un po’ tali attività.