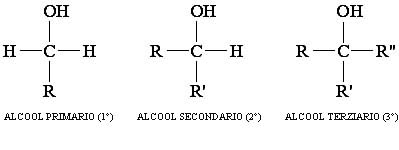
Gli alcoli si classificano in primari, secondari e terziari a seconda se il gruppo funzionale “-OH” è legato ad un carbonio combinato rispettivamente ad uno, due o tre gruppi alchilici come nella figura seguente:
Con il saggio di Lucas è possibile individuare a quale tipo di alcol appartiene il campione da noi testato, ovvero avendo a disposizione un alcol con non più di 6 atomi di carbonio, in quanto deve essere solubile nel reagente di Lucas affinchè il test possa essere eseguito, si può determinare a quale dei tre gruppi questo appartiene.
Il reattivo di Lucas è costituito da cloruro di zinco (ZnCl2) in acido cloridrico (HCl) concentrato e il test si basa sulla velocità di formazione dell’alogenuro alchilico corrispondente che si presenta insolubile.
R-OH + HCl → R-Cl ↓ + H2O
La reazione chimica è una sostituzione nucleofila di tipo1 (SN1). Analizzando il meccanismo di reazione si ha dapprima la protonazione del gruppo -OH dell’alcol che grazie all’azione catalizzante dell’acido lo fa diventare -OH2+ ed in seguito fuoriesce come molecola d’acqua lasciando un carbocatione stabile. Successivamente l’attacco dello ione Cl–, che agisce da nucleofilo, porta alla formazione dell’alogenuto alchilico corrispondente secondo il meccanismo:
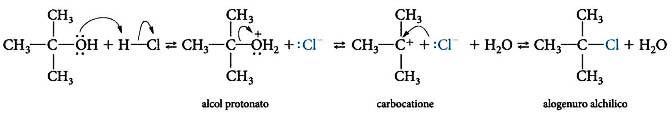
Gli alcoli terziari reagiscono velocemente per formare un alogenuro alchilico in acqua intorbidando la soluzione. La velocità della reazione è regolata dalla possibilità di formazione di un carbocatione terziario che è particolarmente stabile rendendo la carica positiva maggiormente disponibile nel tempo all’attacco del nucleofilo (Cl–). Gli alcoli secondari, che danno luogo alla formazione di un carbocatione secondario, meno stabile di quello terziario, reagirebbero in tempi più lunghi, mentre gli alcoli primari reagiscono in tempi molto lunghi, in quanto si deve ottenere un carbocatione primario che è il meno stabile di tutti e pertanto la soluzione dovrebbe essere anche riscaldata.
Libro consigliato: Link Laboratorio di chimica organica
OBIETTIVO dell’esperienza:
Verificare la presenza di acoli primari, secondari o terziari in un campione.
MATERIALI:
- Provette 16X160mm una per ogni campione da testare;
- Porta provette;
- Pipette Pasteur;
- Cappa aspirante;
- Piastra termica;
- Becher con porta provette per bagnomaria.
REAGENTI:
- Acqua distillata;
- Etanolo, (alcol primario);
- 1-propanolo, (alcol primario);
- Alcol ter-butilico o 2-meti-2-propanolo, (alcol terziario);
- 2-propanolo o isopropanolo, (alcol secondario);
- 2-butanolo, (alcol secondario);
- Reattivo di Lucas costituito da acido cloridrico al 37%(m/m), cloruro di zinco anidro (preparazione: disciogliere in 10 ml
di acido cloridrico concentrato, 16 grammi di cloruro di zinco anidro raffreddando in un bagno di ghiaccio).
VALUTAZIONE DEI RISCHI:
L’esperimento deve avvenire sotto cappa aspirante e adottando i dispositivi di protezione individuale come il camice, occhialetti di protezione e guanti anti acido. Seguire sempre le indicazioni del personale docente esperto. Eliminare gli scarti dei reagenti in appositi recipienti per lo smaltimento dei rifiuti speciali.
PROCEDIMENTO:
- Preparare una serie di provette: una per la prova sicuramente negativa (acqua distillata al posto dell’alcol), una per l’etanolo, una per il 1-propanolo, una per l’alcol 2metil-2-propanolo, una per il 2-propanolo ed una per il 2-butanolo;
- In ogni provetta si introducono 2 ml di reattivo di Lucas;
- Versare 4-5 gocce di alcol nelle rispettive provette precedentemente siglate in modo da riconoscere quale alcol è stato aggiunto;
- Agitare ed osservare eventuali intorbidamenti delle soluzioni;
- Le provette in cui, nell’immediato, non è avvenuto nulla di evidente ad occhio nudo, dovranno essere messe a bagnomaria a caldo per alcuni minuti:
- Annotare i risultati indicando in quali provette è avvenuto un intorbidamento immediato e in quali invece è avvenuto successivamente e in quanto tempo a caldo.

OSSERVAZIONI:
- Nella provetta in cui è stata aggiunta acqua distillata non è avvenuto nulla anche ponendola a caldo;
- Nella provetta contenente 2metil-2propanolo, chiamato anche alcol ter-butilico (alcool terziario), la reazione è pressoché istantanea e si forma il corrispondente alogenuro che intorbida la soluzione;
- Nella provetta in cui è stato aggiunto il 2-propanolo e in quella in cui è stato versato 2-butanolo, (entrambi alcool secondari), la reazione è avvenuta solo dopo aver messo le provette a bagnomaria e dopo qualche minuto;
- Nella provetta con etanolo e in quella del 1-propanolo, gli alcoli si sono semplicemente mescolati con il reattivo senza dar luogo né in tempi brevi né a distanza di ore a formazione evidente di alogenuro pur mantenendoli a caldo.

